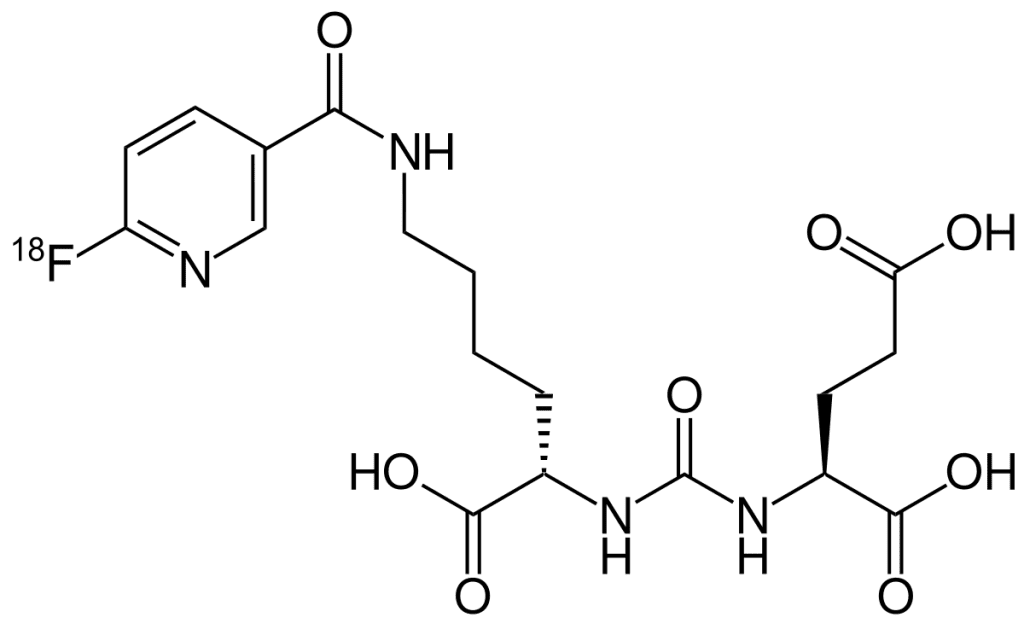
El 24 de julio de 2023 la Agencia Europea del Medicamento (EMA) ha autorizado Pylclari (F-18 piflufolastat) para su utilización en todos los estados miembros de la Unión Europea. La EMA ha considerado que ofrece mejoras sobre los métodos existentes y los efectos adversos fueron leves y su perfil de seguridad aceptable por lo que sus beneficios superan a sus riesgos.
El piflufolastat, también conocido como [F-18] DCFPyL, es un inhibidor del antígeno de membrana específico de próstata (PSMA) marcado con flúor-18 que se une a las células que expresan PSMA. El beneficio de Pylclari es su potencial para diagnosticar el cáncer de próstata en la estadificación primaria de pacientes de alto riesgo y en la estadificación en sospecha de recurrencia en función del aumento del antígeno prostático específico (PSA) en suero, según lo respaldan tres ensayos clínicos prospectivos abiertos.
Pylclari está indicado para la detección de lesiones positivas para PSMA con tomografía por emisión de positrones (PET) en adultos con cáncer de próstata (CaP) en las siguientes situaciones:
- Estadificación primaria de pacientes con CaP de alto riesgo antes de la terapia curativa inicial
- Para localizar recurrencia de CaP en pacientes con sospecha basada en aumento sérico del PSA después del tratamiento primario con intención curativa.
https://www.ema.europa.eu/en/documents/overview/pylclari-epar-medicine-overview_en.pdf
https://www.ema.europa.eu/en/documents/product-information/pylclari-epar-product-information_en.pdf